发布时间:2022.01.05
自身免疫性疾病是一大类慢性炎症性疾病,其主要特征是免疫系统失调和异常活化,对自身抗原的耐受能力降低或丧失,从而导致身体正常组织、器官的免疫损伤和病理。常见的自身免疫性疾病包括系统性红斑狼疮、多发性硬化症、强直性脊柱炎、1型糖尿病、类风湿关节炎等,严重危害身体健康。目前临床治疗药物只能缓解症状、提高患者生活质量和降低病死率,并不能从病因学角度根治疾病。患者不仅需要频繁和终生服药,而且毒副作用大。
调节性T细胞(Treg)是一类具有免疫抑制和调节作用的T细胞亚群,它可以抑制多种免疫细胞亚型的活化、增殖和分化,对维持机体免疫稳态和自身抗原的免疫耐受至关重要,其抑制功能的缺失或受损会导致严重的自身免疫性疾病和慢性炎症。然而,目前并没有针对Treg的药物用于临床治疗自身免疫疾病。
中国科学院微生物研究所的孟颂东团队十多年来长期从事热休克蛋白gp96免疫学功能研究。该团队近期研究发现,高剂量gp96免疫在系统性红斑狼疮Lyn-/-小鼠(SLE)模型中显示了明显的治疗效果,有效降低自身抗体滴度、滤泡辅助性T细胞和产生抗体的浆细胞水平。此外,gp96治疗可减轻小鼠自身免疫性脑脊髓炎(EAE)的发病和进展。机制研究发现gp96处理可显著增加Treg的比例、增殖能力和抑制功能,通过基因表达谱分析发现NF-κB家族成员p65和c-Rel是gp96增强Treg中Foxp3表达的关键转录因子。他们通过构建与Toll样受体(TLRs)结合部位的突变体gp96、TLR2敲除小鼠和Treg细胞特异性缺失MyD88小鼠,均证明gp96通过TLR2-MyD88介导的NF-κB信号通路激活了Treg细胞并诱导Foxp3表达。
该研究阐明了gp96介导的Treg激活的机制,验证了活化的Treg可有效抑制自身抗体和Th细胞诱导的自身免疫性疾病,为研发通过激活Treg治疗自身免疫性疾病的药物提供了依据。鉴于自体gp96蛋白已经用于临床肿瘤治疗并显示出良好的安全性,该团队前期已经建立了天然提取和重组表达gp96蛋白的关键技术,这为设计以gp96蛋白为基础的治疗自身免疫性疾病的新型药物提供了基础。
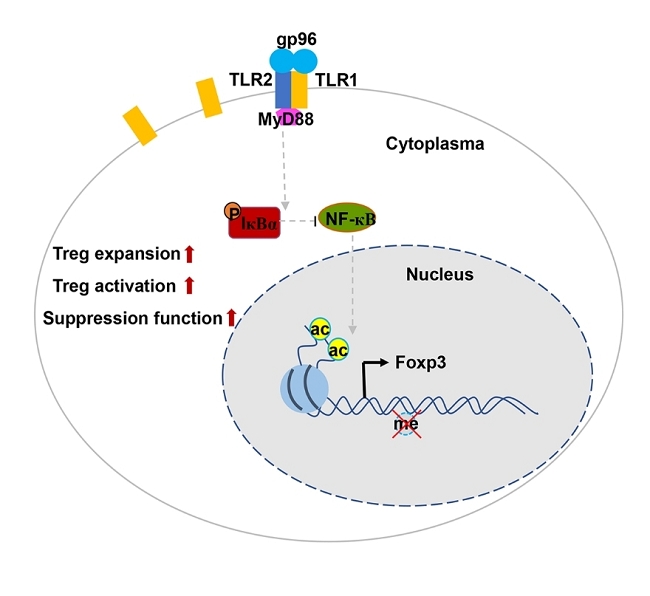
热休克蛋白gp96活化Treg的机制
上述研究成果已于2021年12月在iScience期刊上发表,中国科学院微生物研究所博士生徐玉秀为第一作者,中国科学院微生物研究所孟颂东研究员、研究组的助理研究员李鑫为共同通讯作者。该研究得到了国家自然科学基金和中国科学院战略性先导科技专项(B类)项目的经费支持。
全文链接:https://doi.org/10.1016/j.isci.2021.103445