马超美,女,现任内蒙古大学生命科学院生物系教授。
教育及工作经历:
1998.4-2001.3 日本富山医科药科大学(现与富山大学合并)药学博士
1996.4-1998.3 日本富山医科药科大学(现与富山大学合并)药学硕士
1979.9-1983.7 北京医学院药学系(现北京大学药学院)学士
2010.5- 内蒙古大学生命科学院生物系 教授
2006.7-2010.3 日本富山大学和汉医药学综合研究所 副教授
2003.3-2006.7 加拿大纽芬兰记念大学药学院 博士后
2001.5-2003.3 北京大学药学院 讲师-副教授
1994.4-1996.3 日本富山医科药科大学和汉药研究所 世川研修生-客员研究员
1983.8-1994.3 内蒙古医学院药学系 助教-讲师
主讲课程:
资料更新中……
培养研究生情况:
养博士生6名,硕士生12名。
招聘信息:
本室招收博士后,工资按在岗讲师待遇发放。
液-质联用UPLC-QQQMS (Agilent 1290-6430)可对外测试全扫描质谱、未知样品LC-MS/MS定性分析、已知样品LC-MRM定量分析等。
研究方向:
天然药物与功能食品研究
研究领域:
1.植物成分的提取、分离和结构测定。
如:锁阳(Cynomorium songaricum)、文冠木(Xanthoceras sorbifolia)等中蒙药的生物活性成分研究。
2.植物成分衍生物及类似物的合成和生物活性研究。
如:绿原酸衍生物和类似物的制备及生物活性,三萜类化合物的结构改造及生物活性等。
3.植物成分体内外代谢研究。
如:生物碱的体内代谢产物的结构测定等。
承担科研项目情况:
先后承担国家自然科学基金,内蒙古自然科学基金,内蒙古科技厅基金,内蒙古大学科研启动基金,中国博士后科学基金,国家大学生创新基金项目。
科研成果:
资料更新中……
发表论文:
2015
1. Bulgantuya Bumandorj; Narantsetseg Byambaakhuu; 叶日贵; 岳丽丽; 何小丽; 马超美 红花的抗氧化活性成分研究 内蒙古大学学报(自然科学版) 2015-05-15
2. 张慧文; 许海燕; 马超美 花生红衣研究进展 优先出版 花生学报 2015-02-13
3. 许海燕; 何小丽; 张麟; 赵敏; 杨勇智; 柴绍华; 马超美 锁阳膳食纤维的制备及其物理性质 食品与生物技术学报 2015-01-15
2014
4. 叶日贵; 高杰; 王冰; 李二虎; 张燕; 江飞; 曹瑞; 服部征雄; 王世明; 马超美 超高效液相-串联四极杆质谱联用法同时测定并比较甘草各部位中8种成分含量 食品科学 2014-10-25
5. 张慧文; 张玉; 马超美 原花青素的研究进展 优先出版 食品科学 2014-08-25
6. 王晓琴; 王力伟; 赵岩; 马超美 广枣的化学成分和药理活性研究进展 优先出版 食品科学 2014-08-25
7. 冀敏; 李淑娟; 马超美 窄叶蓝盆花花序化学成分及其抗氧化和抑制α-葡萄糖苷酶活性的研究 优先出版 内蒙古大学学报(自然科学版) 2014-07-04
2013
8. Zhang, H. W.; Yerigui, Yang, Y. M.; Ma, C. M. Structures and Antioxidant and Intestinal Disaccharidase Inhibitory Activities of A-Type Proanthocyanidins from Peanut Skin. J Agric Food Chem 61: 8814−8820 (2013).
9. Zhang, L.; Li, M. Y.; Wang, L. W.; Gao, J.; Ma, C. M. Isolation, Identification, Quantification and Inhibitory Activity on HCV Protease of Coumarins from Viola yedoensis. Can Chem Trans 1: 157-164 (2013).
10. Hattori, M.; Ma, C. M., Wei, Y.; El Dine, R. S.; Sato, N. Survey of Anti-HIV and Anti-HCV Compounds from Natural Sources. Can Chem Trans 1: 116-140 (2013).
11. 麻剑南, 何倩倩, 王雅丽, 马超美. 苹果皮有效成分及药理作用研究进展. 食品与药品 15: 219-222 (2013).
12. Meng, H. C.; Wang, S.; Li, Y.; Kuang, Y. Y.; Ma, C. M. Chemical constituents and pharmacologic actions of Cynomorium plants. Chin J Nat Med 11: 0321−0329 (2013).
13. Meng, H. C.; Ma, C. M. Flavan-3-ol-cysteine and acetylcysteine conjugates from edible reagents and the stems of Cynomorium songaricum as potent antioxidants. Food Chem 141: 2691-2696 (2013).
14. Wang, W.; He, X. L.; Ma, C. M. Metabolism schemes of chlorogenic, quinic and caffeic acid derivatives in rats deduced by molecular fragments detected with optimized UPLC–APCI-MS/MS. Int J Mass Spectrom 337: 34–42 (2013).
15. Gao, J.; Sato, N.; Hattori, M.; Ma, C. M. The simultaneous quantification of Ganoderma acids and alcohols using ultra performance liquid chromatography-mass spectrometry with dynamic selected reaction monitoring mode. J Pharm Biomed Anal 74: 246-249 (2013).
2012
16. Wu, Z. G.; Xu, H. Y.; Ma, Q.; Cao, Y.; Ma, J. N.; Ma, C. M. Isolation, identification and quantification of unsaturated fatty acids, amides, phenolic compounds and glycoalkaloids from potato peel. Food Chem 135: 2425–2429 (2012). ISSN: 0308-8146
17. Ma, J. N.; Wang, S. L.; Zhang, K.; Wu, Z. G.; Hattori, M; Chen, G. L.; Ma, C. M. Chemical components and antioxidant activity of the peels of commercial apple-shaped pear (fruit of Pyrus pyrifolia cv. pingguoli), J Food Sci 77: 1097–1102 (2012). Online ISSN: 1750-3841.
18. Jin, J. S., Tobo, T., Chung, M. H., Ma, C. M.; Hattori, M. Transformation of trachelogenin, an aglycone of tracheloside from safflower seeds, to phytoestrogenic (−)-enterolactone by human intestinal bacteria. Food Chem 134: 74-80 (2012).
19. Kitalong, C.; El-Halawany, A. M.; El-Dine, R. S.; Ma, C. M.; Hattori, M. Phenolics from Phaleria nisidai with estrogenic activity. Rec Nat Prod 6: 296-300. (2012).
20. Zhong, Y.; Ma, C.M.; Shahidi, F. Antioxidant and antiviral activities of lipophilic epigallocatechin gallate (EGCG) derivatives. J Funct Food 4: 87-93. (2012).
21. Wang, Z. G.; Wang, X. J.; Sun, H.; Chen, L.; Ma, C. M. Determination of novel nitrogen-containing metabolite after oral administration of swertiamarin to rats. J Asian Nat Prod Res. 14 (2): 176-181 (2012).
22. 危英, 马超美, 梁光义, 魏升华, 危莉, 服部征雄. 民族药野梦花基源及提取物抗丙型肝炎病毒NS3/4A蛋白酶活性研究. 时珍国医国药 23: 1661-1663 (2012).
2011
23. Nakamura, K.; Nishihata, T.; Jin, J-S.; Ma, C. M.; Komatsu, K.; Iwashima, M.; Hattori, M. The C-glucosyl bond of puerarin was cleaved hydrolytically by a human intestinal bacterium strain PUE to yield its aglycone daidzein and an intact glucose. Chem Pharm bull 59: 23-27 (2011).
2010
24. Ma, C. M; Abe, T.; Komiyama, T.; Wang, W.; Hattori, M.; Daneshtalab, M. Synthesis, anti-fungal and 1,3-ß-D-glucan synthase inhibitory activities of caffeic and quinic acid derivatives. Bioorg Med Chem 18: 7009-7014 (2010).
25. Ma, C. M.; Kawahata, T.; Hattori, M.; Otake, T.;Wang, L.; Daneshtalab, M. Synthesis, anti-HIV and anti-oxidant activities of caffeoyl 5,6-anhydroquinic acid derivatives. Bioorg Med Chem 18: 863-869 (2010).
26. Ma, C. M.; Sato, N.; Li, X. Y.; Nakamura, N.; Hattori, M. Flavan-3-ol contents, anti-oxidative and a-glucosidase inhibitory activities of Cynomorium songaricum. Food Chem 118: 116-119 (2010).
27. Wang, W.; Ma, C. M.; Hattori, M. Metabolism and Pharmacokinetics of Rhynchophylline in Rats. Bio Pharm Bull 33: 669-676 (2010).
28. Wang, W.; Ma, C. M.; Hattori, M. Metabolism of isorhynchophylline in rats detected by LC-MS.JPPS 13: 27-37 (2010).
29. Wang, W.; Ma, C. M.; Hattori, M. Simultaneous determination of rhynchophylline, isorhynchophylline, and their eight metabolites in rats. J Trad Med 27: 15-29 (2010).
30. 赵建荣; 尚明英; 孟立强; 容嵩; 马超美; 屈磊; 蔡少青; 李晓玫 黄芪当归合剂肾脏保护作用的有效部位筛选 中国中药杂志 2010-11-01
31. 王如峰; 杨秀伟; 马超美; 蔡少青; 徐暾海 金莲花脂肪酸成分研究 中药材 2010-10-25
32. Dong, S. W.; Wang, X.; Shang, M.Y.; Ma, C. M.; Zhang, S. X.; Li, X. W.; Xu, M. J.; Cai, S. Q.; Namba, T. Sesquiterpene and Aristolochic Acid Derivatives from Thottea hainanensis, Helvetica Chimica Acta: 354-360 (2010).
33. Wang, J.; Chung M. H.; Xue B.; Ma H.; Ma, C. M.; Hattori, M. Estrogenic and Antiestrogenic Activities of Phloridzin. Bio Pharm Bull 33,592-597 (2010).
2009
34. Ma, C. M.; Wu, X. H.; Hattori, M.; Wang, X. J.; Kano, Yoshihiro. HCV protease inhibitory, cytotoxic and apoptosis-inducing effects of oleanolic acid derivatives. JPPS. 12: 243-248 (2009).
35. Ma, C. M.; Wei, Y.; Wang, Z. G.; Hattori, M. Triterpenes from Cynomorium songaricum—analysis of HCV protease inhibitory activity, quantification, and content change under the influence of heating. J Nat Med 63: 9-14 (2009).
36. El Dine, R. S.; El Halawany, A. M.; Ma, C. M.; Hattori, M. Inhibition of the dimerization and active site of HIV-1 protease by secondary metabolites from the Vietnamese mushroom Ganoderma colossum. J Nat Prod. 72: 2019-23 (2009).
37. Sato, N.; Zhang, Q.; Ma, C. M.; Hattori, M. Anti-HIV-1 protease activity of new lanostain-type triterpenoids from Ganoderma sinense. Chem Pharm Bull 57: 1076-1080 (2009).
38. Zhang, Q.; Zuo, F.; Nakamura, N.; Ma, C. M.; Hattori, M. Metabolism and pharmacokinetics in rats of ganoderiol F, a highly cytotoxic and antitumor triterpene fromGanoderma lucidum. J Nat Med 63: 304-310 (2009).
39. Wei, Y.; Ma, C. M.; Hattori, M. Synthesis and evaluation of A-seco type triterpenoids for anti-HIV-1 protease activity. Eur J Med Chem 44: 4112-4120 (2009).
40. Sato, N.; Ma, C. M.; Komatsu, K.; Hattori, M. Triterpene-farnesyl hydroquinone conjugates from Ganoderma sinense. J Nat Prod 72: 958-961 (2009).
41. Wei, Y.; Ma, C. M.; Hattori, M. Synthesis of dammarane-type triterpene derivatives and their ability to inhibit HIV and HCV proteases. Bioorg Med Chem 17: 3003-3010 (2009).
42. Wei, Y.; Ma, C. M.; Hattori, M. Anti-HIV protease triterpenoids from the acid hydrolysate of Panax ginseng. Phytochemistry Letters 2: 63-66 (2009).
43. Phuong, D. T.; Ma, C. M.; Hattori, M.; Jin, J. S. Inhibitory Effects of Antrodins A-E from Antrodia cinnamomea and Their Metabolites on Hepatitis C Virus Protease. Phytother Res 23: 582-584 (2009).
44. Yu, J,; Ma, C. M.; Long, C. F.; Wang, X.; Shang, M. Y.; Cai, S. Q.; Hattori, M.; Namba, T. A new aristololactam from Asarum maximum. Journal of Chinese Pharmaceutical Sciences 18: 183–185 (2009).
2008
45. Ma, C. M.; Hattori, M.; Daneshtalab, M.; Wang, L. Chlorogenic Acid Derivatives with Alkyl Chains of Different Lengths and Orientations: Potent a-Glucosidase Inhibitors. J Med Chem 51: 6188-6194 (2008).
46. Ma, C. M.; Hattori, M.; Chen, H. B.; Cai, S.-Q.; Daneshtalab, M. Profiling the Phenolic Compounds of Artemisia pectinata by HPLC-PAD-MSn. Phytochem Analysis 19: 294-300 (2008).
47. Xu, Q.; Ma, C. M.; Wang, W.; Fu, X.; Tang C. Y.; Hattori, M. Study on the nitric oxide generating effects from aristolochic acid in vitro. Eur J Mass Spectrom 14: 231-238(2008).
48. Wei Y; Ma, C. M.; Chen D. Y; Hattori M. Anti-HIV-1 protease triterpenoids fromStauntonia obovatifoliola Hayata subsp. intermedia. Phytochemistry 69: 1875-1879 (2008).
49. Wang, Z. G.; Ma C. M.; Tang, S. H.; Xiao, H,; Kakiuchi, N.; Kida, H.; Hattori, M. Qualitative and Quantitative Analysis of Swertia Herbs by High Performance Liquid Chromatography-Diode Array Detector-Mass Spectrometry (HPLC-DAD-MS). Chem Pharm Bull 56: 485-490 (2008).
50. Lee, J. S.; Ma, C. M.; Hattori, M. Quantification of ergosterol and ergosterol peroxide in several medicinal fungi by high performance liquid chromatography monitored with a diode array detection-atmospheric pressure chemical ionization-ion trap mass spectrometer. J Trad Med25: 18-23 (2008).
51. Lee, J. S.; Ma, C. M.; Park, D. K.; Yoshimi, Y.; Hatanaka, M.; Hattori, M. Transformation of ergosterol peroxide to cytotoxic substances by rat intestinal bacteria. Bio Pharm Bull 31: 949-54 (2008).
52. Tang, S. H.; Wang, Z. G.; Ma C. M.; Hattori, M. Simultaneous determination of ten bioactive constituents in Eucommia ulmoides leaves and Tochu tea products by high-performance liquid chromatography-diode array detector-mass spectrometry (HPLC-DAD-MS). J Trad Med 25: 112-118 (2008).
53. El Dine, R. S.; El Halawany, A. M.; Ma, C. M.; Hattori, M. Anti-HIV-1 Protease Activity of Lanostane Triterpenes from the Vietnamese Mushroom Ganoderma colossum. J. Nat. Prod.71: 1022-1026 (2008).
54. Wang, Z. G.; Tang, S. H.; Ma C. M.; Toyooka,N.; Kida, H.; Kawasaki,M.; Hattori, M. Determination of novel nitrogen-containing metabolites after oral administration of swertiamarin to rats. J Trad Med25: 29-34 (2008).
55. El Dine, R. S.; El Halawany, A. M.; Nakamura, N.; Ma, C. M.; Hattori, M. New lanostane triterpene lactones from the Vietnamese mushroom Ganoderma colossum (FR.) C. F. BAKER. Chem Pharm Bull 56: 642-646 (2008).
2007
56. Ma, C. M.; Kully, M.; Khan, J. K.; Hattori, M.; Daneshtalab, M. Synthesis of chlorogenic acid derivatives with promising antifungal activity. Bioorg Med Chem. 15: 6830-6833 (2007).
57. Ma, C. M.; Winsor, L.; Daneshtalab, M. Quantification of spiroether isomers and herniarin of different parts of Matricaria matricarioides and flowers of Chamaemelum nobile. Phytochem Analysis. 18:42-49 (2007).
58. 杨秀伟; 赵静; 马超美; 服部征雄 七叶树皂苷和熊果酸类化合物对HIV-1蛋白酶活性抑制作用的初步研究 中国新药杂志 2007-03-08
59. El-Halawany, A. M.; Chung, M. H.; Ma, C. M.; Komatsu, K.; Nishihara, T.; Hattori, M. Anti-estrogenic activity of mansorins and mansonones from the heartwood of Mansonia gagei DRUMM.Chem Pharm Bull 55: 1332-1337 (2007).
2006
60. Ma, C. M.; Takeda, S.; Hibino, S.; Daneshtalab, M. Synthesis of peptidomimetic analogues of echinocandins. Heterocycles, 68: 721-732, (2006).
2005
61. Ma, C. M.; Cai, S. Q.; Cui, J. R.; Wang, R. Q.; Tu, P. F.; Hattori, M.; Daneshtalab, M. The cytotoxic activity of ursolic acid derivatives. Eur J Med Chem 40: 582-589 (2005).
62. 侴桂新; 中村宪夫; 马超美; 王峥涛; 服部征雄 乌药中异喹啉类生物碱(英文) 中国天然药物 2005-09-20
2004
63. Ma, C. M.; Nakamura, N.; Nowawi, A.; Hattori, M.; Cai, S. Q. A Novel Protoilludane Sesquiterpene from the Wood of Xanthoceras sorbifolia. Chin Chem Lett 15: 65-67 (2004).
64. Loomis, T. G.; Ma, C. M.; Daneshtalab, M. Medicinal plants and herbs of Newfoundland. Part 1. Chemical constituents of the aerial part of Pineapple weed (Matricaria matricarioides). Daru 12: 131-135 (2004).
65. 赵建荣; 屈磊; 马超美; 李晓玫 黄芪当归合剂肾保护作用的药效部位及其机制研究 “中华医学会肾脏病学分会2004年年会”暨“第二届全国中青年肾脏病学术会议”论文汇编 2004-06-30
2003
66. 王如峰; 杨秀伟; 马超美; 尚明英; 杨珊; 王闽川; 蔡少青 胖大海中脂肪酸成分的气-质联用分析 中国中药杂志 2003-06-25
2002
67. 马超美, 中村宪夫, 服部征雄, 蔡少青. 锁阳的抗艾滋病毒蛋白酶活性成分(2)-齐墩果酸丙二酸半酯的分离和鉴定. 中国药学杂志 37: 336-338 (2002).
68. Ma, C. M.; Nakamura, N.; Hattori, M.; Kawahata, T.; Otake, T. Inhibitory effects of triterpene-azidothymidine conjugates on proliferation of human immunodeficiency virus type 1 and its protease. Chem Pharm Bull 50: 877-880 (2002).
69. Ma, C. M.; Nakamura, N.; Miyashiro, H..; Hattori, M.; Komatsu, K.; Kawahata, T.; Otake, T. Screening of Chinese and Mongolian herbal drugs for anti-human immunodeficiency virus type 1 (HIV-1) activity. Phytother Res 16: 186-189 (2002).
2001
70. Ma, C. M.; Nakamura, N.; Min, B. S.; Hattori, M.Triterpenes and lignans from Artemisia caruifolia and their cytotoxic effects on Meth-A and LLC tumor cell lines. Chem Pharm Bull 49: 183-187 (2001).
71. Ma, C. M.; Nakamura, N.; Mattori, M. Inhibitory effects on HIV-1 protease of tri-p-coumaroylspermidine from Artemisia caruifolia and related amides. Chem Pharm Bull 49: 915-917 (2001).
2000
72. Ma, C. M.; Nakamura, N.; Hattori, M.; Kakuda, H.; Qiao, J. C.; Yu, H.L.; Inhibitory effects on HIV-1 protease of constituents from the wood of Xanthoceras sorbifolia. J Nat Prod 63: 238-242 (2000).
73. Ma, C. M.; Nakamura, N.; Hattori, M.; Z. S.; Komatsu, K. Guaiane dimers and germacranolide from Artemisia caruifolia. J Nat Prod 63: 1626-1629 (2000).
74. Ma, C. M.; Nakamura N.; Hattori, M.Chemical modification of oleanene type triterpenes and their inhibitory activity against HIV-1 protease dimerization. Chem Pharm Bull 48: 1681-1688 (2000).
2000年以前的
75. Ma, C. M.; Nakamura, N.; Miyashiro, H.; Hattori M.; Shimotohno, K.Inhibitory effects of constituents from Cynomorium songaricum and related triterpene derivatives on HIV-1 protease. Chem Pharm Bull 47: 141-145 (1999).
76. Nawawi, A.; Ma, C. M.; Nakamura, N.; Hattori, M.; Kurokawa, M.; Shiraki, K.; Kashiwaba N.; Ono, M. Anti-herpes simplex virus activity of alkaloids isolated from Stephania cepharantha. Bio Pharm Bull 22: 268-274 (1999).
77. Kawata, Y.; Ma, C. M.; Meselhy, M. R.; Nakamura, N.; Wang, H.; Hattori, M.; Namba, T.; Satoh, K.; Kuraishi, Y. Conversion of aconitine to lipoaconitine by human intestinal bacteria and their antinociceptive effects in mice. J Trad Med 16: 15-23 (1999).
78. 桂新; 李庆林; 王峥涛; 徐珞珊; 徐国钧; 中村宪夫; 马超美; 服部征雄 乌药活性组分LEF的化学成分及抗风湿作用 植物资源与环境 1999-10-30
79. Ma, C. M.; Nakamura, N.; Hattori, M. Saponins and C-glycosyl flavones from the seeds of Abrus precatorius. Chem Pharml Bull 46: 982-987 (1998).
80. 杨秀伟; 赵静; 张雁; 李建新; 马超美; 服部征雄; 难波恒雄 大黄的研究 Ⅰ.秦岭大黄中一个新的丙二酸单酰基蒽醌糖苷化合物 中草药 1998-05-15
81. Lim, Y. A.; Ma, C. M.; Kusumoto, I. T.; Miyashiro, H.; Hattori, M.; Gupta, M. P.; Correa, M. HIV-1 reverse transcriptase inhibitory principles from Chamaesyce hyssopifolia. Phytother Res 11: 22-27 (1997).
82. Ma, C. M.; Miyashiro H, Hattori M, Shimotohno K. Screening of Chinese and Mongolian traditional medicines for the inhibitory activity on human immunodeficiency virus type 1 protease. J Trad Med 12: 418-419 (1995).
83. 马超美, 贾世山, 孙韬, 张义文. 锁阳中三萜及甾体成分的研究. 药学学报 28: 152-5 (1993)
84. Jia, S. S.; Ma, C. M.; Li, Y. H.; Hao, J. H. Glycosides of phenolic acid and flavonoids from the leaves of Glycyrrhiza uralensis Fisch. 药学学报 27: 441-4 (1992). (CT 5)
85. Jia, S. S.; Ma, C. M.; Jan-Min Wang, study on the flavonoid constituents from the aerial part ofGlycyrrhiza uralesis. 药学学报 25: 758-762 (1990). (CT 4)
86. Jia, S. S.; Ma, C. M.; Zhao, L. F. Aliphatic constituents from the pollen of Typha angustifolia L. 植物学报 32: 465-8 (1990).
87. 贾世山; 刘永漋; 马超美; 杨世林; 周慧敏; 赵达成; 刘冬; 李淑玉 狭叶香蒲花粉(蒲黄)黄酮类成分的研究药学学报 1986-06-30
荣誉奖励:
资料更新中……
博士后:王伟博士(复旦大学硕士,日本富山大学博士,昆明医科大学药学院副教授 副院长,内蒙古大学在职博士后,中国博士后面上基金及特别资助获得者),
Olusegun Ajala博士(尼日利亚拉格斯大学博士,讲师,内蒙古大学博士后,中国博士后“中非伙伴计划”资助获得者)
博士生:张慧文,布拉干图雅,王玲娜,宝乐日,阿吉吉雅,高杰
硕士生:何小丽,冀敏,其其格,麻剑南,王雅丽,张轲,许海燕,马琼,
张玉,叶日贵,武志刚(与本院王迎春教授研究室合作培养生)。

内蒙古大学天然药物与功能食品研究室建立于2010年,主要从事内蒙古优势植物及特色蒙药材有效成分的研究,团队带头人为马超美教授。为了提供民族天然药物活性成分的化学结构及生物活性的科学数据,进一步扩大民族天然药物的国际化,为了建立天然药物的质量控制方法确保和优化天然药物的治疗效果,天然药物与功能食品团队对一些中蒙药的有效成分结构、定性定量方法及生物活性进行了研究。另外,由于天然药物的生物活性成分本身在国内外同样受到越来越多的重视,导致其来源中蒙药材的需求量增加,中药材种植的土地资源日益短缺。为了能够变废为宝,扩大生物活性成分提取资源,团队对食品加工副产物的成分及活性进行了研究。通过对内蒙古特色优势植物及食品加工副产物中有效成分的提取纯化、结构改造、生物活性、定性定量分析及体内代谢等方面进行研究,取得了诸多创新成果。
1 提取分离鉴定天然药物及食品加工副产物的活性成分
本着“药食同源”的思路,团队不仅对纯药材还对一些食品加工副产物的活性成分进行了研究。一些果蔬的外皮常含有植物为防卫自身受到病害侵犯而产生的二次代谢产物(成分),这些成分也可能对人体防御疾病有效。因此团队的研究内容之一是从含果蔬外皮的食品加工副产物中找到无毒或毒性小并有丰富来源的有效成分。
1.1 文冠木等蒙药材及花生红衣的原花青素类成分
蒙古族的传统饮食以高脂肪高蛋白的奶、肉为主,易形成包括中心性肥胖、高血压、高血脂、脂肪肝和II型糖尿病等临床表现的代谢综合症。为了预防和治疗这些疾病,蒙古民族使用了一些特色药材。团队主要成员前期研究发现蒙药材文冠木中含有A型原花青素类成分。花生红衣为花生加工副产品,除了少量在中医药中用于治疗慢性出血和支气管炎外,绝大多数被丢弃掉。团队用多种色谱法从花生红衣中分离得到10个原花青素类化合物,经各种光谱法和化学降解法证明了其结构,其中包括新化合物及首次从花生中分离得到的化合物。发现有些红衣成分具有很强的清除自由基活性和中等程度的抑制α-葡萄糖苷酶活性的作用。α-葡萄糖苷酶抑制剂通过延迟肠道碳水化合物的吸收来控制餐后高血糖,临床上使用的α-葡萄糖苷酶抑制剂代表性药物是阿卡波糖。研究结果提示花生红衣原花青素类成分可能对II型糖尿病及肥胖症的防治有帮助。
1.2 内蒙古自治区优势水果的果皮成分
对内蒙古自治区优势水果苹果梨和123果(金红苹果)的果皮进行了系统的活性成分研究。发现这些果皮含有熊果酸等多种三萜成分,并含有酚类成分,包括首次从苹果属和梨属植物中发现的酚类成分。这些果皮有很强的抗氧化活性,其中的多酚和缩合鞣质的含量也比其果肉部分更高。已知熊果酸有保肝、抗癌和抗病毒等生物活性,还可作为先导化合物合成抗癌、抗病毒试剂。苹果梨和123果皮中三萜成分特别是熊果酸的含量丰富,可作为提取高价值活性成分的原料。研究的果皮中高价值活性成分的分离、纯化和含量测定方法,为开发基于果汁加工副产物——果渣及果皮的功能食品、药品或化妆品奠定了坚实基础。
1.3 土豆皮的生物活性成分
内蒙古自治区是土豆的主要产区。通常,人们在制作土豆菜肴或工业化制作薯片薯条时将皮去除,其中部分被用作饲料,但每年仍有大量的土豆皮被弃掉。据文献报道土豆皮有治疗烫伤、降低血压等作用。然而,土豆皮中的龙葵碱等生物碱成分可抑制人体胆碱酯酶从而引起食物中毒。课题组从土豆皮中分离纯化出酚酸、不饱脂肪酸、生物碱糖苷和酰胺类成分,鉴定出两个少见的不饱和三羟基脂肪酸,其中1个含有Omega-3 不饱和脂肪酸结构。以Omega-3不饱和脂肪酸为有效成分的深海鱼油因有防治心血管疾病,防治老年痴呆、增进专注力和舒解压力等效果而广为人知,而土豆皮中的Omega-3 不饱和脂肪酸是否有同样功效值得进一步研究,其开发利用也值得期待。团队的研究为将土豆皮有毒的龙葵碱等成分部分与药用成分部分分开,将有效部分制成药物或功能食品,将含龙葵碱的有毒部分试制成低污染的植物源杀虫剂打下基础。
1.4 紫花地丁的生物活性成分
紫花地丁是治疗肝病的蒙药复方的组成药材,团队从紫花地丁中提取得到的双香豆素化合物具有很强的活性抑制丙型肝炎蛋白酶活性,是该药材在中医及蒙医中用于肝病的活性物质基础之一。
2 天然产物的结构改造
2.1 锁阳低分子鞣质–半胱氨酸缩合物
锁阳具有强身健体作用,主产于为我国西北荒漠地区。课题组通过用食用试剂处理锁阳,制备纯化出黄烷-3-醇类化合物的半胱氨酸结合物和乙酰半胱氨酸结合物,包括新化合物,证明这些结合物均有更高的清除游离基作用,有些还有抑制小肠二糖酶等α-葡萄糖苷酶作用,有可能开发成为具有辅助降血糖作用的功能食品。由锁阳分别制备出锁阳三萜提取物及锁阳黄烷-3-醇-半胱氨酸缩合物的方法简单易行,成本低,无毒性,分别可用于制备保肝保健食品或药品和具有高抗氧化活性的功能食品和药品。
2.2 儿茶素和表儿茶素的部分乙酰化物及丙酮缩合物
团队制备了儿茶素和表儿茶素的部分乙酰化物及丙酮缩合物,包括新化合物,证明二乙酰化物和丙酮缩合物有很好的清除游离基作用,并能穿透细胞膜进入活细胞内,因而有望发挥更好的体内效果,也可能作为低极性食品、化妆品等的抗氧化剂。
2.3 绿原酸类似物及衍生物
绿原酸是具有清除自由基、抗氧化、抗病毒等重要生理活性的天然产物,对II-型糖尿病、心血管疾病及一些和衰老有关的疾病等有预防或治疗作用。绿原酸的含量被国家药典指定为判断金银花等重要药材的质量标准。课题组制备了以酰胺键代替酯键的绿原酸衍生物,其体内外稳定性比绿原酸大幅提高,有望发挥更好的药效。团队还制备了绿原酸组成单元——咖啡酸和奎宁酸的衍生物,证明有些衍生物具有抗深部真菌作用,部分作用机理是由于抑制真菌细胞壁合成的1,3-β-葡萄糖苷酶作用引起的。
3 天然药物活性成分的定量分析和代谢研究
3.1 灵芝等真菌的成分分析及其辅助抑制癌细胞作用 灵芝是重要的中药材,然而其有效成分含量受各种因素的影响很大。灵芝三萜是灵芝的主要有效成分,具有抑制癌细胞生长、保肝、抑制艾滋病毒蛋白酶活性等作用,被认为是灵芝发挥疗效的活性物质基础。课题组建立了同时测定8种灵芝三萜酸和三萜醇的超高效液相色谱–串联四极杆质谱联用法,为灵芝药材及其复方的质量控制提供了参考。另外,课题组体外实验发现,灵芝及其他药用和食用真菌的麦角甾醇过氧化物成分与紫杉醇合用,可提高对一些癌细胞的选择性杀伤力,减少紫杉醇的用量。
3.2 天然药物活性成分的体内代谢 研究了具有抗真菌作用的绿原酸、咖啡酸和奎宁酸的酰胺衍生物的体内代谢过程,发现绿原酸衍生物在体内会转化为奎宁酸衍生物,绿原酸衍生物和咖啡酸衍生物还会发生其它代谢反应,而奎宁酸衍生物在体内的稳定性好;红花种子中得到的络石甙元在肠内细菌作用下可以转化为植物雌激素——肠内酯;这些活性成分的体内代谢和生物转化研究结果为解释其体内作用机理和新药设计提供了重要参考。
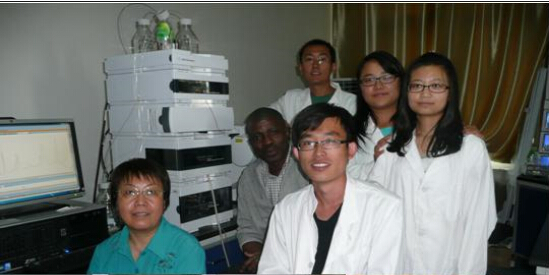
团队学术交流

团队风采:

中国科技创新人物云平台暨“互联网+”科技创新人物开放共享平台(简称:中国科技创新人物云平台)免责声明:
1、中国科技创新人物云平台是:“互联网+科技创新人物”的大型云平台,平台主要发挥互联网在生产要素配置中的优化和集成作用,将互联网与科技创新人物的创新成果深度融合于经济社会各领域之中,提升实体经济的创新力和生产力,形成更广泛的以互联网为基础设施和实现工具的经济发展新形态,实现融合创新,为大众创业,万众创新提供智力支持,为产业智能化提供支撑,加快形成经济发展新动能,促进国民经济提质增效升级。
2、中国科技创新人物云平台暨“互联网+”科技创新人物开放共享平台内容来源于互联网,信息都是采用计算机手段与相关数据库信息自动匹配提取数据生成,并不意味着赞同其观点或证实其内容的真实性,如果发现信息存在错误或者偏差,欢迎随时与我们联系,以便进行更新完善。
3、如果您认为本词条还有待完善,请编辑词条。
4、如果发现中国科技创新人物云平台提供的内容有误或转载稿涉及版权等问题,请及时向本站反馈,网站编辑部邮箱:kjcxac@126.com。
5、中国科技创新人物云平台建设中尽最大努力保证数据的真实可靠,但由于一些信息难于确认不可避免产生错误。因此,平台信息仅供参考,对于使用平台信息而引起的任何争议,平台概不承担任何责任。

















