研究方向:免疫遗传学
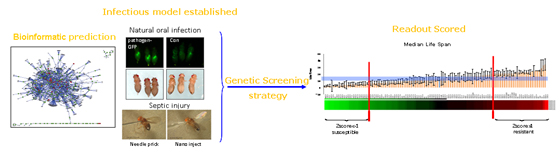
1. 天然免疫系统是生物机体抵抗病源入侵的第一道防线,有着极其重要的作用,并在进化中保持着高度的保守性。果蝇由于拥有精细复杂的天然免疫系统,便利快捷的遗传操作手段,已经成为研究天然免疫系统和模拟高等动物感染的理想疾病模型。因此我们拟建立一系列果蝇遗传筛选体系,寻找参与天然免疫调节的新因子,新通路和新机制,加深天然免疫同其他生理病理通路之间的网络调控机制的理解, 以期能够更好的从机体的整体水平上掌控天然免疫的调控机理,解决困扰人类的多种天然免疫相关问题,增强我们抵抗病原微生物感染的能力。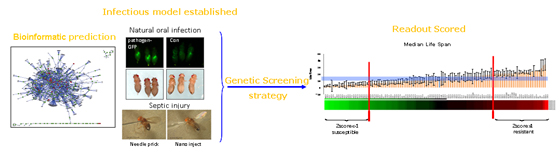
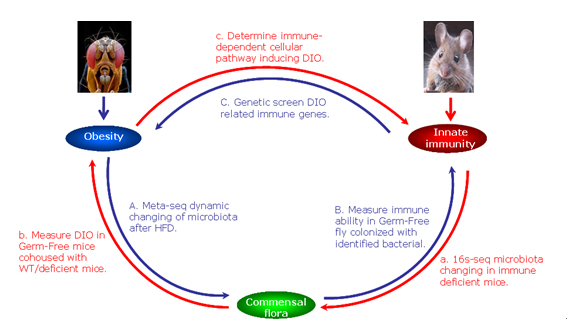
2. 高热量/脂肪饮食(WTD)导致体重增加和肥胖(DIO)与肠道菌群-肠道免疫互作有关,但免疫应答与调控规律不详。我们拟利用果蝇和肠道免疫缺陷小鼠两种模型各自的优势,联合研究DIO过程中(1)肠道菌群稳态以及能量和脂肪代谢变化规律;(2)影响肠道菌微生态和宿主能量与脂肪代谢的免疫调节机制,以期确定肠道粘膜免疫、肠道菌群和肥胖症之间的网络调控关系,揭示DIO的肠道生态免疫学应答与调控的分子与细胞机制。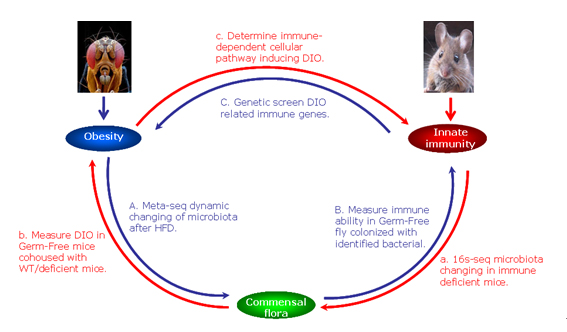
承担科研项目情况:
1 .国家自然基金青年基金(31000403) 主持 2011-2013
2. “十二五”艾滋病和病毒性肝炎等重大传染病防治科技重大专项(2012ZX10001006) 子课题负责人 2012-2015
3. 973重要传染病基础研究专项(2012CB518900) 研究骨干 2012-2016
4. 科技部国家国际科技合作专项(2011DFG32790) 研究骨干 2012-2014
5. 中国科学院-诺和诺德联合研究项目 (NNCAS-2011-2) 主持 2012-2013
6. 国家自然基金重大国际(地区)合作交流项目(81220108018) 中方课题负责人 2013-2017
7. 973重要传染病基础研究专项(2012CB117289) 研究骨干 2013-2017
8. 国家自然基金面上项目(31370909) 主持 2014-2017
研究成果:
资料更新中......
出版专著:
《Nature》发表唐宏研究组潘磊副研究员和Stowers研究所关于干细胞命运调控新机制的合作研究
2014年8月6日,《Nature》杂志在线发表了唐宏研究组潘磊副研究员和美国解亭教授实验室的合作研究论文“Protein competition switches the function of COP9 from self-renewal to differentiation”,揭示了蛋白因子之间的竞争性结合调控干细胞自我更新和分化的新机制。
干细胞在发育过程中主要经历两种命运抉择:一是自我更新的增殖过程;一是转变为功能性子代细胞的分化过程。如何精确的调控干细胞在适当的发育阶段行使正确的命运选择一直是干细胞研究领域所关注的重点问题。既要保证干细胞为机体提供源源不断的具有功能的子代分化细胞;又要保证干细胞在其微环境中存有足够的储备。同时,既要防止干细胞过度分化所造成的干细胞储备库的枯竭;又要避免干细胞过分增殖所引发的肿瘤样结构。因此,深入的了解如何平衡干细胞自我更新-分化之间的转变对于人们掌握干细胞的调控机制乃至更好的利用干细胞的医疗价值有着重要的意义。
我们在多年的研究中发现干细胞自身调节因子和来源于微环境的信号因子共同控制着干细胞的发育命运。不像多数的微环境信号因子具有一定的影响范围,很多干细胞自身调节因子广泛的分布在干细胞和其后续分化的子代细胞中。这不禁就产生了一个有趣的问题,这些广泛表达的调节因子是如何转变其在干细胞中的维持更新能力到子代细胞中的促分化能力的?我们选用果蝇的卵巢种系干细胞作为研究模型,结合遗传学,生物化学和细胞生物学等多种研究手段,提出了一种调控干细胞的新机制。在干细胞中,Csn4因子作为COP9复合物的一份子维持干细胞的自我更新;而在分化的子代在细胞中,大量表达的促分化因子Bam通过竞争性募集Csn4,从而转变其他的Csn蛋白组分发挥促进分化的功能。同时,余下的Bam将进一步和另一个蛋白因子Bgcn结合形成促进干细胞分化的复合体,并抑制自我更新因子的表达。这种通过调节因子之间的竞争性结合从而转变功能的机制可能很好的解释了在多种干细胞体系中虽然干细胞和其子代拥有共同的调节因子但却拥有不同命运的现象。
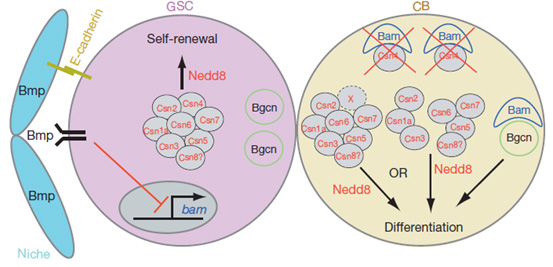
图示果蝇种系干细胞通过蛋白竞争结合的调控机制
该论文是继双方合作发表多篇阐述干细胞调节机制的文章后(Cell Stem Cell 2007,COLD SPRING HARB SYM.2008,PLoS genetics 2011,Developmental Cell 2014)所提出的关于干细胞命运调控的全新理论。其中中国科学院生物物理研究所感染与免疫院重点实验室的潘磊副研究员是本文的第一作者。美国Stowers研究所的解亭教授作为本文通讯作者。该研究受科技部973(to L.P.),国家基金委(to L.P.),NIH(to T.X.)和Stowers(to T.X.)研究所的资助,在中国科学院生物物理研究所,Stowers研究所和清华大学共同完成。
发表英文论文:
1. Pan L, Chen S, Weng C, Call G, Zhu D, Tang H, Zhang N, Xie T. Stem Cell Aging Is Controlled Both Intrinsically and Extrinsically in the Drosophila Ovary. Cell stem cell, 2007, 1:458-469 (Faculty 1000 factor=6,cited 85)
2. Xie T, Song X, Jin Z, Pan L, Weng C, Chen S, Zhang N. Interactions between Stem Cells and Their Niche in the Drosophila Ovary. COLD SPRING HARB SYM.2008, 73:39-47
3. Yu J*, Pan L*, Qin X, Chen H, Xu Y, Chen Y and Tang H. MTMR4 attenuates TGFβ signaling by dephosphorylating R-Smads in endosomes. The Journal of biological chemistry 2010, 285(11):8454-62. (*co-first author)
4. Wang X*, Pan L*, Wang S*, Zhou J, McDowell W, Park J, Haug J, Staehling K, Tang H, Xie T. Histone H3K9 Trimethylase Eggless Controls Germline Stem Cell Maintenance and Differentiation. PLoS genetics 2011, 7(12): e1002426. (*co-first author)
5. Zhang X, Weng C, Li Y, Wang X, Jiang C, Li X, Xu Y, Chen Q, Pan L* and Tang H*. Human Bop is a novel BH3-only member of the Bcl-2 protein family. Protein & Cell 2012, 3 (10): 790–801 (* Correspondence author)
6. Yu J, He X, Chen Y, Hao Y, Yang S, Wang L, Pan L* and Tang H*. Myotubularin-related protein 4 (MTMR4) attenuates BMP/Dpp signaling by dephosphorylation of Smad proteins. The Journal of biological chemistry 2013, 288 (1): 79-88 (* Correspondence author)
7. Yan D, Neumuller RA, Buckner M, Ayers K, Li H, Hu Y, Yang ZD, Pan L, Wang X, Kelley C, Vinayagam A, Binari R, Randklev S, Perkins LA, Xie T, Cooley L, and Perrimon N. A Regulatory Network of Drosophila Germline Stem Cell Self-Renewal. Developmental Cell 2014, 28, 459–473. (Resource article)
8. Chen J, Zhao Y, Zhang C, Chen H, Feng J, Chi X, Pan Y, Du J, Guo M, Cao H, Chen H, Wang Z, Pei R, Wang Q, Pan L, Niu J, Chen X, Tang H. Persistent hepatitis C virus infections and hepatopathological manifestations in immune-competent humanized mice. Cell Research, 2014;doi:10.1038
9. Pan L, Wang S, Lu T, Weng C, Song X, Park J, Sun J, Yang Z, Yu J, Tang H, McKearin D, Chamovitz D, Ni J, Xie T. Protein competition switches the function of COP9 from self-renewal to differentiation. NATURE, 2014; doi:10.1038/nature13562